المفروض (أ)الأيثان ول و(ب)ايثير ثنائى الميثيل
المناهج الجديدة 2018 / 2019 :
|
|
المفروض (أ)الأيثان ول و(ب)ايثير ثنائى الميثيل
حل السؤال الأول بالصور
الصور المرفقة

حل السؤال الثانى
الصور المرفقة

عذرا ولكن هذا هو السؤال كامل
الصور المرفقة

الف شكر يا مستر ع المجهود الرائع
السؤال الأول أ) إختر كل إختيار عليه درجة ( 6 × 1 = 6 درجات )إجابات إمتحان الكيمياء دور أول 2010
1) [ب] السلسلة الإنتقالية الثالثة
2) [ ﺟ ] النشادر
3) [ أ ] HF
4) [ د ] 1 فاراداي
5) [ ب ] طاقة تظهر على هيئة خطوط طيفية
6) [ أ ] 3
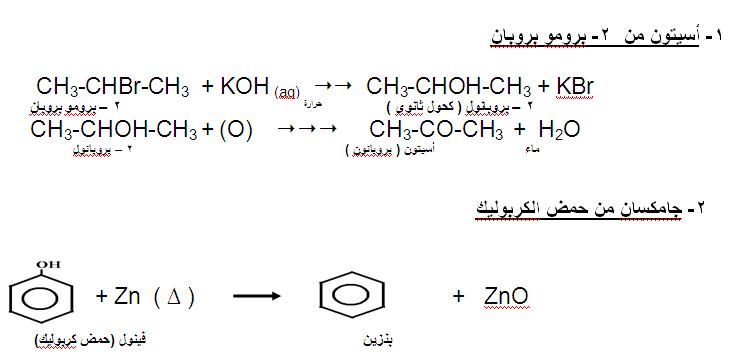
ب) 1- أسيتون من 2- برومو بروبان درجتان كل خطوة درجة
2 – بروبانول ( كحول ثانوى ) حرارة 2 – برومو بروبانCH3-CHOH-CH3 + KBr¢ CH3-CHBr-CH3 + KOH (aq)
ماء أسيتون ( بروبانون ) 2 – بروبانول أيزوبروبان ولCH3-CHOH-CH3 + (O) ¢ CH3-CO-CH3 + H2O
2- جامكسان من حمض الكر***يك درجتان كل خطوة درجة
[IMG]file:///D:/DOCUME%7E1/bbbbb/LOCALS%7E1/Temp/msohtml1/01/clip_image 003.gif[/IMG]
+ ZnO ( ∆ ) Zn +
بنزين فينول (حمض كر***يك)
[IMG]file:///D:/DOCUME%7E1/bbbbb/LOCALS%7E1/Temp/msohtml1/01/clip_image 005.jpg[/IMG]
إجابة السؤال الثاني أ ) الإسم الكيميائي [ على ما أظن كل صيغة نصف درجة ]
1) [ 3- إيثيل -1- هكساين ]
2) [ 2- فينيل بروبان ]
3) [ 3,2- ثنائي ميثيل بيوتانويك ]
4) [ إستر بروبانوات الفينيل ]
ب) 1)
P2 (NH3) ( 0.6 ) 2
Kp = ــــــــــ ــــــــــ ــــــــــ ـــــ = ــــــــــ ــــــــــ ــــــــــ ــــــ = 4.3732 × 10 ــ 4
P3 (H2) . ( N2 ) (7.1 )3 × ( 2.3 )
التعليق : قيمة Kp صغيرة جدأ وهذا يعني أن التفاعل نشط في الإتجاه العكسي
2) الترتيب حسب قيمة pH [ CH3COONa > NaCl > NH4Cl]
ﺟ) 1-
العنصر
التوزيع الالكتروني
الفئة
ﺟ الكلورالفئة ( P )(10Ne) 3S2 , 3P5
د البوتاسيومالفئة ( S )(18Ar) 4S1
2- الرابطة الآيونية تنشأ بين العنصرين ( ﺟ , د )
الرابطة التساهمية النقية تنشأ بين ذرتين من العنصر ( أ )
الرابطة التساهمية القطبية تنشأ بين العنصرين ( أ , ﺟ )
3- المركب هو الإيثين ونوع التهجين ( SP2 )
د) 1- العلاقة ( n2 ) مربع رقم المستوي الأساسي
2- لأن الغازات الناتجة من عملية الإختزال وهى (CO2 , H2O) يتم تبريدها وتنقيتها ثم
إمرارها مع كمية أخرى من الغاز الطبيعى على العامل الحفز لينتج خليط من الغازات
المختزلة ( CO , H2 ) مرة أخرى
إجابة السؤال الثالث أ)
3 - فى الإتزان التالى CH3COOH + H2O ⇌ CH3COO - + H3O +
وضح تأثير كل من التغيرات التالية على تركيز أيون الأسيتات
أ ) إضافة قطرات من حمض الهيدروكلو ريك
ب ) إضافة قطرات من محلول هيدروكسيد الصوديوم
أ ) عند إضافة قطرات من حمض الهيدروكلو ريك يزداد تركيز آيون الهيدروجين الموجب والذى يرتبط مع جزئالإجابة
الماء برابطة تناسقية مكونا ً آيون الهيدرونيو م أى يقل تركيز الماء ويزداد تركيز آيونات الهيدرونيو م فينشط
الإتزان فى الإتجاه العكسى أى يقل تركيز آيون الأسيتات ( CH3COO - )
ب) عند إضافة قطرات من محلول هيدروكسيد الصوديوم يزداد تركيز آيون الهيدروكسي د السالب والذى يتحد مع
آيون الهيدرونيو م مكونا ً جزيئين ماء أى يزداد تركيز الماء ويقل تركيز آيونات الهيدرونيو م فينشط الإتزان
فى الإتجاه الطردى أى يزداد تركيز آيون الأسيتات ( CH3COO - )
ب) علل
(1) لأن عدد الروابط الهيدروجين ية بين كل جزيئين من الحمض الكربوكسيل ي ضعف عدد الروابط الهيدروجين ية بين كل جزيئين كحول
(2) كلوريد حديد ІІІ مادة بارامغناطي سية بسبب وجود خمسة إلكترونات مفردة فى أوربيتالات المستوى الفرعى (3d) ينتج عن دورانها مجالات مغناطيسية تتجاذب مع المجال المغناطيسي الخارجي و كلوريد الخارصين مادة ديا مغناطيسية بسبب إزدواج جميع إلكترونات (3d)
(3) لأن النحاس يلي الهيدروجين في متسلسلة الجهود الكهربية أي أقل نشاط من الهيدروجين بينما الصوديوم في مقدمة المتسلسلة فهو أنشط من الهيدروجين
(4) لأن الطاقة الناتجة عن إزدواجه مع آخر أقل من الطاقة اللازمة لإنتقاله إلى مستوى أعلى
ﺟ) 1) أولا ً بإضافة ملح كربونات صوديوم إلى عينة من كل منها
في حالة حدوث فوران وتصاعد غاز يعكر ماء الجير الرائق يكون المحلول لحمض الأسيتيك
بينما في حالة الفينول والإيثانول لا يحدث شئ
ثم نضيف محلول مائي للتفرقة بين الفينول والإيثانول
في حالة تلون المحلول باللون البنفسجي يكون المحلول فينول
بينما الإيثانول لا يحدث تفاعل
2) أ- الكروم في طلاء المعادن لحمايتها من الصدأ
ب) عدد أفوجادرو لمعرفة عدد الجزيئات أو الذرات أو الآيونات الموجودة في مولات من المادة
السؤال الأول أ) إختر كل إختيار عليه درجة ( 6 × 1 = 6 درجات )إجابات إمتحان الكيمياء دور أول 2010
1) [ب] السلسلة الإنتقالية الثالثة
2) [ ﺟ ] النشادر
3) [ أ ] HF
4) [ د ] 1 فاراداي
5) [ ب ] طاقة تظهر على هيئة خطوط طيفية
6) [ أ ] 3
ب) 1- أسيتون من 2- برومو بروبان درجتان كل خطوة درجة
2 – بروبانول ( كحول ثانوى ) حرارة 2 – برومو بروبانCH3-CHOH-CH3 + KBr¢ CH3-CHBr-CH3 + KOH (aq)
ماء أسيتون ( بروبانون ) 2 – بروبانول أيزوبروبان ولCH3-CHOH-CH3 + (O) ¢ CH3-CO-CH3 + H2O
2- جامكسان من حمض الكر***يك درجتان كل خطوة درجة
[IMG]file:///D:/DOCUME%7E1/bbbbb/LOCALS%7E1/Temp/msohtml1/01/clip_image 003.gif[/IMG]
+ ZnO ( ∆ ) Zn +
بنزين فينول (حمض كر***يك)
[IMG]file:///D:/DOCUME%7E1/bbbbb/LOCALS%7E1/Temp/msohtml1/01/clip_image 005.jpg[/IMG]
إجابة السؤال الثاني أ ) الإسم الكيميائي [ على ما أظن كل صيغة نصف درجة ]
1) [ 3- إيثيل -1- هكساين ]
2) [ 2- فينيل بروبان ]
3) [ 3,2- ثنائي ميثيل بيوتانويك ]
4) [ إستر بروبانوات الفينيل ]
ب) 1)
P2 (NH3) ( 0.6 ) 2
Kp = ــــــــــ ــــــــــ ــــــــــ ـــــ = ــــــــــ ــــــــــ ــــــــــ ــــــ = 4.3732 × 10 ــ 4
P3 (H2) . ( N2 ) (7.1 )3 × ( 2.3 )
التعليق : قيمة Kp صغيرة جدأ وهذا يعني أن التفاعل نشط في الإتجاه العكسي
2) الترتيب حسب قيمة pH [ CH3COONa > NaCl > NH4Cl]
ﺟ) 1-
العنصر
التوزيع الالكتروني
الفئة
ﺟ الكلورالفئة ( P )(10Ne) 3S2 , 3P5
د البوتاسيومالفئة ( S )(18Ar) 4S1
2- الرابطة الآيونية تنشأ بين العنصرين ( ﺟ , د )
الرابطة التساهمية النقية تنشأ بين ذرتين من العنصر ( أ )
الرابطة التساهمية القطبية تنشأ بين العنصرين ( أ , ﺟ )
3- المركب هو الإيثين ونوع التهجين ( SP2 )
د) 1- العلاقة ( n2 ) مربع رقم المستوي الأساسي
2- لأن الغازات الناتجة من عملية الإختزال وهى (CO2 , H2O) يتم تبريدها وتنقيتها ثم
إمرارها مع كمية أخرى من الغاز الطبيعى على العامل الحفز لينتج خليط من الغازات
المختزلة ( CO , H2 ) مرة أخرى
إجابة السؤال الثالث أ)
3 - فى الإتزان التالى CH3COOH + H2O ⇌ CH3COO - + H3O +
وضح تأثير كل من التغيرات التالية على تركيز أيون الأسيتات
أ ) إضافة قطرات من حمض الهيدروكلو ريك
ب ) إضافة قطرات من محلول هيدروكسيد الصوديوم
أ ) عند إضافة قطرات من حمض الهيدروكلو ريك يزداد تركيز آيون الهيدروجين الموجب والذى يرتبط مع جزئالإجابة
الماء برابطة تناسقية مكونا ً آيون الهيدرونيو م أى يقل تركيز الماء ويزداد تركيز آيونات الهيدرونيو م فينشط
الإتزان فى الإتجاه العكسى أى يقل تركيز آيون الأسيتات ( CH3COO - )
ب) عند إضافة قطرات من محلول هيدروكسيد الصوديوم يزداد تركيز آيون الهيدروكسي د السالب والذى يتحد مع
آيون الهيدرونيو م مكونا ً جزيئين ماء أى يزداد تركيز الماء ويقل تركيز آيونات الهيدرونيو م فينشط الإتزان
فى الإتجاه الطردى أى يزداد تركيز آيون الأسيتات ( CH3COO - )
ب) علل
(1) لأن عدد الروابط الهيدروجين ية بين كل جزيئين من الحمض الكربوكسيل ي ضعف عدد الروابط الهيدروجين ية بين كل جزيئين كحول
(2) كلوريد حديد ІІІ مادة بارامغناطي سية بسبب وجود خمسة إلكترونات مفردة فى أوربيتالات المستوى الفرعى (3d) ينتج عن دورانها مجالات مغناطيسية تتجاذب مع المجال المغناطيسي الخارجي و كلوريد الخارصين مادة ديا مغناطيسية بسبب إزدواج جميع إلكترونات (3d)
(3) لأن النحاس يلي الهيدروجين في متسلسلة الجهود الكهربية أي أقل نشاط من الهيدروجين بينما الصوديوم في مقدمة المتسلسلة فهو أنشط من الهيدروجين
(4) لأن الطاقة الناتجة عن إزدواجه مع آخر أقل من الطاقة اللازمة لإنتقاله إلى مستوى أعلى
ﺟ) 1) أولا ً بإضافة ملح كربونات صوديوم إلى عينة من كل منها
في حالة حدوث فوران وتصاعد غاز يعكر ماء الجير الرائق يكون المحلول لحمض الأسيتيك
بينما في حالة الفينول والإيثانول لا يحدث شئ
ثم نضيف محلول مائي للتفرقة بين الفينول والإيثانول
في حالة تلون المحلول باللون البنفسجي يكون المحلول فينول
بينما الإيثانول لا يحدث تفاعل
2) أ- الكروم في طلاء المعادن لحمايتها من الصدأ
ب) عدد أفوجادرو لمعرفة عدد الجزيئات أو الذرات أو الآيونات الموجودة في مولات من المادة
اجابة امتحان الكيمياء
السؤال الاول
1- ب
2- ج
3- أ
4- د
5- ب
6- أ
التح***ة
1- (هيدروكسيد صوديوم تسخين) ---------ايزوبروبيل ى-------(اكسده بالبرنجنات المحمضة )---------
2- تسخين فى وجود الزنك ---------------بنزين ----------------(كلورة فى ضوء الشمس المباشر)------
السؤال الثاني
3- إيثيل هكساين
2- فينيل بروبان
2و3 ثنائى ميثيل بيوتانويك
بروبانوات الفينيل
التعليق هو التفاعل نشط فى العكسى (ضغوط المتفاعلات أكبر)
النتيجة
4.37x 10-3
اعلها فى الأس الهيدروجين ى اسيتات صوديوم
***يها كلوريد صوديوم
يليها كلوريد امونيوم
ج-
هيدروجين كربون كلور بوتاسيوم العناصر (مش طلبها للتوضيح)
1- ج ود عناصر ممثلة الفئة (27a) p والفئة s (1a
2- رابطة ايونية ج مع د
تساهمية نقية زرتين من ج او من أ
تساهمية قطبية أ مع ج
3- الايثيلين ونوع التهجين sp2
السؤال الثالث
1- يزداد تركيز أيون الهيدرونيو م (نظرا لزيادة الهيدروجين الموجب الناتج من تأين الهيدروكلو ريك ) ويسير التفاعل فى الأتجاة العكسي على حسب لوشاتيليه ويقل تركيز ايون الأسيتات
2- يتحد أيون الهيدروكسي ل الناتج من تاين هيدروكسيد الصوديوم مع الهيدروجين (الهيدروني وم ) فيتم سحب الهيدروجين ويسير التفاعل فى الأتجاة الطردي على حسب لوشاتيليه ويزداد تركيز ايون الأسيتات
التمييز
1- نستخدم fecl3
فى حالة الفينول لون بنفس** والباقى -
وللتمييز بين الأيثانول والأسيتك
2- بيكربونات الصوديوم
فى حالة فوران ----- الأستيك
السؤال الرابع
1- (أ) الأيثانول و (ب) ايثير ثنائى الميثيل
2- 2الأيثانول --------( كبريتيك 140) ------- ايثير ثنائى الأثيل
3- الأيثانول مع الصوديوم ------- ايثو...... ...+ هيدوجين
1- التمييز fecl3
احمردموى (ثيو سيانات)
بنى محمر (هيدروكسيد)
2- بوضح نقطتين من حمص الهيدروكلو ريك (اي حمض)
و ذكر الألوان وكذلك أى قاعدة و زكر الألوان
الخامس
1- اختزال الحمض ب 2 جزىء هيدروجين يتحول الى كحول (الشروط كرومات النحاس عند 200)
2- يتفاعل مع كحول لتح*** لأستر (hcl dry) تم التحلل النشادرى



شكرااااااا اااااااااا ااااا


شكرا جزيلا
المفضلات